Аминокислоты 
Общую формулу простейших аминокислот можно записать так:
Н2N— СН—СООН
I
R
Так как аминокислоты содержат две различные функциональные группы, которые оказывают влияние друг на друга, их реакции отличаются от характерных свойств карбоновых кислот и аминов.
Получение
Аминокислоты можно получить из карбоновых кислот, заместив в их радикале атом водорода на галоген, а затем на аминогруппу при взаимодействии с аммиаком. Смесь аминокислот обычно получают кислотным гидролизом белков.
Свойства
Аминогруппа —NН2 определяет основные свойства аминокислот, так как способна присоединять к себе катион водорода по донорно-акцепторному механизму за счет наличия свободной электронной пары у атома азота.
Группа —СООН (карбоксильная группа) определяет кислотные свойства этих соединений. Следовательно, аминокислоты — это амфотерные органические соединения.
Со щелочами они реагируют как кислоты. С сильными кислотами — как основания-амины.
Кроме того, аминогруппа в молекуле аминокислоты вступает во взаимодействие с входящей в ее состав карбоксильной группой, образуя внутреннюю соль:
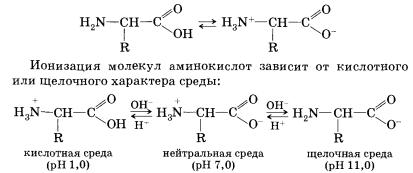
Так как аминокислоты в водных растворах ведут себя как типичные амфотерные соединения, то в живых организмах они играют роль буферных веществ, поддерживающих определенную концентрацию ионов водорода.
Аминокислоты представляют собой бесцветные кристаллические вещества, плавящиеся с разложением при температуре выше 200 °С. Они растворимы в воде и нерастворимы в эфире. В зависимости от состава радикала R— они могут быть сладкими, горькими или безвкусными.
Аминокислоты обладают оптической активностью, так как содержат атомы углерода (асимметрические атомы), связанные с четырьмя различными заместителями (исключение составляет амино-уксусная кислота — глицин). Асимметрический атом углерода обозначают звездочкой.
Как вы уже знаете, оптически активные вещества встречаются в виде пар антиподов-изомеров, физические и химические свойства которых одинаковы, за исключением одного — способности вращать плоскость поляризованного луча в противоположные стороны. Направление вращения плоскости поляризации обозначается знаком (+) — правое вращение, (-) — левое вращение.
Различают D-аминокислоты и L-аминокислоты. Расположение аминогруппы NH2 в проекционной формуле слева соответствует L-конфигурации, а справа — D-конфигурации. Знак вращения не связан с принадлежностью соединения к L- или D-ряду. Так, L-ce-рин имеет знак вращения (-), а L-аланин — (+).
Аминокислоты подразделяют на природные (обнаруженные в живых организмах) и синтетические. Среди природных аминокислот (около 150) выделяют протеиногенные аминокислоты (около 20), которые входят в состав белков. Они представляют собой L-формы. Примерно половина из этих аминокислот относятся к незаменимым, так как они не синтезируются в организме человека. Незаменимыми являются такие аминокислоты, как валин, лейцин, изолейцин, фени-лалалин, лизин, треонин, цистеин, метионин, гистидин, триптофан. В организм человека данные вещества поступают с пищей (табл. 7). Если их количество в пище будет недостаточным, нормальное развитие и функционирование организма человека нарушаются. При отдельных заболеваниях организм не в состоянии синтезировать и некоторые другие аминокислоты. Так, при фенилкетонурии не синтезируется тирозин.
Важнейшим свойством аминокислот является способность вступать в молекулярную конденсацию с выделением воды и образованием амидной группировки—NH—СО—, например:
H2N—(СН2)5—СООН + Н—NH—(СН2)5—СООН —>
аминокапроновая кислота
—+ H2N—(СН2)5—СО—NH—(СН2)5—СООН + Н20 димер
Получаемые в результате такой реакции высокомолекулярные соединения содержат большое число амидных фрагментов и поэтому получили название полиамидов.
К ним, кроме названного выше синтетического волокна капрон, относят, например, и энант, образующийся при поликонденсации аминоэнантовой кислоты. Для получения синтетических волокон пригодны аминокислоты с расположением амино- и карбоксильной групп на концах молекул (подумайте почему). Таблица 7. Суточная потребность организма человека в аминокислотах

Полиамиды а-аминокислот называются пептидами. В зависимости от числа остатков аминокислот различают дипептиди, трипептиды, полипептиды. В таких соединениях группы —NР—СО— называют пептидными.
Изомерия и номенклатура
Изомерия аминокислот определяется различным строением углеродной цепи и положением аминогруппы. Широко распространены также названия аминокислот, в которых положения аминогруппы обозначаются буквами греческого алфавита. Так, 2-аминобутановую кислоту можно назвать также а-аминомасляной кислотой:
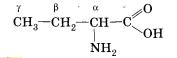
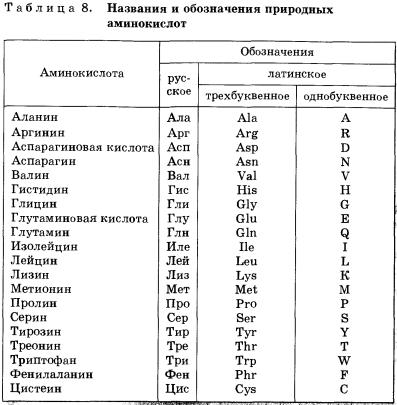
В биосинтезе белка в живых организмах участвуют 20 аминокислот, для которых применяют чаще исторические названия. Эти названия и принятые для них русские и латинские буквенные обозначения приведены в таблице 8.
1. Запишите уравнения реакций аминопропионовой кисло-; ты с серной кислотой и гидроксидом натрия, а также с метиловым спиртом. Всем веществам дайте названия по международной номенклатуре.
2. Почему аминокислоты являются гетерофункциональными соединениями?
3. Какими особенностями строения должны обладать аминокислоты, используемые для синтеза волокон, и аминокислоты, участвующие в биосинтезе белков в клетках живых организмов?
4. Чем отличаются реакции поликонденсации от реакций полимеризации? В чем их сходство?
5. Как получают аминокислоты? Запишите уравнения реакций получения аминопропионовой кислоты из пропана.
6. Определите строение а-аминокислоты, если известно, что она содержит 15,73% азота.
7*. Смесь массой 30 г, содержащая аминоуксусную кислоту и уксусный альдегид, для солеобразования требует 5,38 л хлороводорода (н. у.) или 10,08 г оксида кальция. Определите массовые доли веществ в исходной смеси.
| 






