Ферменты Ферменты, или энзимы, — это органические катализаторы белковой природы, которые ускоряют реакции, необходимые для функционирования живых организмов.
Так как реакции обмена веществ, протекающие в организмах, можно разделить на два типа процессов: синтеза (анаболические) л распада (катаболические), то соответственно можно выделить и два типа ферментов. Примером анаболического фермента может служить глутаминсинтетаза. Примером катаболического фермента может служить мальтаза.
Сейчас химикам известно более 2000 ферментов. Все они обладают рядом специфических свойств, отличающих их от неорганических катализаторов.
Размер молекул. Понятно, что, будучи по своей природе белками, ферменты должны иметь большие значения молекулярной массы. Действительно, она может колебаться в пределах от 105 до 107, а это значит, что по своему размеру молекулы ферментов попадают в разряд коллоидных частиц. Это не позволяет отнести их ни к гомогенным, ни к гетерогенным катализаторам. Остается отнести их к особому классу катализаторов.
Селективность. Каждый фермент ускоряет только одну какую-либо реакцию или группу однотипных реакций. Эту их особенность называют селективностью (избирательностью) действия. Она позволяет организму быстро и точно выполнить четкую программу синтеза нужных ему соединений на основе молекул пищевых веществ или продуктов их превращения. Располагая богатым набором ферментов, клетка разлагает молекулы белков, жиров и углеводов до небольших фрагментов-мономеров (аминокислот, глицерина и жирных кислот, моносахаридов соответственно) и из них заново строит белковые и иные молекулы, которые будут точно соответствовать потребностям данного организма. Недаром великий русский физиолог, нобелевский лауреат И. П. Павлов назвал ферменты носителями жизни.
Эффективность. Большинство ферментов обладает очень высокой эффективностью. Скорость некоторых ферментативных реакций может быть в 1015 раз больше скорости реакций, протекающих в их отсутствие. Такая высокая эффективность ферментов объясняется тем, что их молекулы в процессе «работы» очень быстро восстанавливаются (регенерируют). Типичная молекула фермента может регенерировать миллионы раз за минуту, например, широко используемый в сыроделии фермент реннин способен вызывать коагуляцию (свертывание) белков молока в количествах, в миллионы раз превышающих его собственную массу. Этот фермент вырабатывается слизистой оболочкой особого отдела желудка жвачных животных — сычуга.
А вот еще один пример высокой эффективности «работы» фермента, хорошо знакомого вам из курса химии 8 класса, — катала-зы. За одну секунду при температуре, близкой к точке замерзания воды, одна молекула этого вещества разлагает около 50 000 молекул пероксида водорода:
каталаза
2Н202----------> 2Н20 + 02
Этот катализатор снижает энергию активации от 75 кДж/моль до 21 кДж/моль. Для сравнения укажем, что если для ускорения этой реакции применяется платина, находящаяся в коллоидном состоянии, то энергия активации понижается только до 50 кДж/моль. Что же такое энергия активации? Представим себе смесь бензина и кислорода. Реакция между этими двумя веществами возможна, но она не пойдет без затраты некоторого количества энергии, поступившей, например, в форме простой искры. Вот такая энергия, которая необходима для того, чтобы вещества начали взаимодействовать между собой, и называется энергией активации. Чем больше требуемая энергия активации, тем ниже скорость реакции при данной температуре. Ферменты, действуя как катализаторы, снижают энергию активации, которая требуется для того, чтобы могла произойти реакция. Они повышают общую скорость реакции, не изменяя в какой-нибудь значительной степени температуру, при которой эта реакция протекает. Аналогично «работают» и неорганические катализаторы, но они уступают в эффективности ферментам.
Зависимость от температуры. Многие ферменты обладают наибольшей эффективностью при температуре человеческого тела, т. е. приблизительно при 37 °С. Человек погибает при более низких и более высоких температурах не столько из-за того, что его убила болезнь, а в первую очередь из-за того, что перестают действовать ферменты, а следовательно, прекращаются обменные процессы, которые и определяют сам процесс жизни. Неорганические катализаторы сохраняют активность в более широком интервале температур. Вспомните, например, синтез аммиака, который проводят при температуре 450—500 °С (катализатор — железо).
Зависимость от среды раствора. Ферменты наиболее эффективно действуют на субстрат при строго определенной среде раствора, при определенных значениях так называемого рН. Величина рН, как показано на схеме, характеризует кислотность и основность растворов и может принимать значения от 1 до 14.
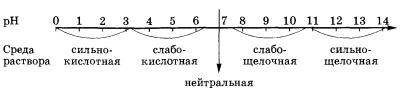
Фермент желудочного сока пепсин наиболее активен при рН 1,5—2 (сильнокислая среда), каталаза крови — при рН 7 (нейтральная среда) и т. д.
Кислотность или основность среды физиологических жидкостей определяет биологическую активность клеток организма, которая, в свою очередь, определяется «работой» действующих в них ферментов (табл. 12). Каждая из физиологических жидкостей имеет определенное значение рН, и отклонение от нормы может быть причиной тяжелых заболеваний.
Таблица 12. Значения рН физиологических жидкостей
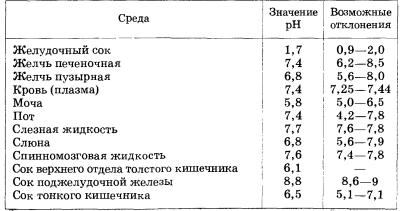
Более подробно с водородным показателем рН вы будете знакомиться в курсе химии следующего года обучения. Пока же вспомните многочисленные телевизионные ролики, в которых вовсю эксплуатируется понятие рН (в них его называют рН-фактор) в рекламных целях.
В контакт с субстратом вступает лишь очень небольшая часть молекулы фермента, так называемый активный центр. Он включает обычно от 3 до 15 аминокислотных остатков полипептидной молекулы фермента. Высокая специфичность фермента обусловлена особой формой его активного центра, которая точно соответствует форме молекулы вещества катализируемой реакции. Их можно сравнить с «ключом и замком»: катализируемое вещество выступает в роли «ключа», который точно подходит к «замку», т. е. к ферменту.
Многие ферменты для проявления активности нуждаются в веществах небелковой природы — так называемых кофакторах. В роли последних могут выступать ионы металлов (цинка, марганца, кальция и др.) или молекулы органических соединений; в последнем случае их называют коферментажи. Иногда для действия фермента бывает необходимо присутствие как ионов металла, так и коферментов.
В некоторых случаях кофермент очень прочно соединен с белком, например у каталазы, где кофермент представляет собой комплексное соединение железа с белком — гемоглобин.
В других ферментах коферменты представляют собой вещества, близкие к витаминам, которые являются предшественниками коферментов. Например, из витамина Вх (тиамина) в клетках образуется тиаминпирофосфат — кофермент важного фермента, входящего в группу декарбоксилаз; из витамина В12 образуются коферменты, необходимые для усвоения жирных кислот с нечетным числом атомов углерода.
Как же классифицируют ферменты?
В 1961 г. специальной комиссией Международного биохимического союза была предложена систематическая номенклатура ферментов. Согласно этой номенклатуре ферменты были поделены на шесть групп в соответствии с общим типом реакции, которую они катализируют. Каждый фермент при этом получил систематическое название, точно описывающее катализируемую им реакцию. Однако, поскольку многие из этих систематических названий оказались очень длинными и сложными, каждому ферменту было также присвоено и тривиальное, рабочее название, предназначенное для повседневного употребления. В большинстве случаев оно состоит из названия вещества, на которое действует фермент, указания на тип катализируемой реакции и окончания -аза (табл. 13).
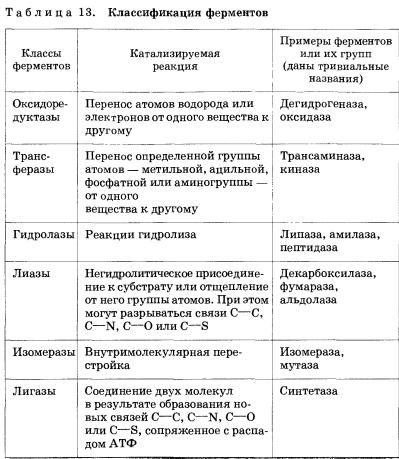
Значение ферментов невозможно переоценить. Только в человеческом организме ежесекундно происходят тысячи и тысячи ферментативных химических реакций. Вспомним хотя бы те, с которыми вы знакомились на уроках биологии в теме «Пищеварение». Например, фермент амилаза, который содержится в слюне (его еще называют птиалином) и в соке тонкого кишечника, помогает превращению крахмала в мальтозу. Затем мальтоза превращается в глюкозу в тонком кишечнике с помощью другого фермента — малъ-тазы. В желудке и тонком кишечнике такие ферменты, как пепсин и трипсин, превращают белки в более простые соединения — пептиды. Затем эти пептиды превращаются в тонком кишечнике в аминокислоты под действием ферментов, которые, понятно, называются пептидазами. А вот на жиры (липиды) в тонком кишечнике действует фермент липаза, расщепляющий их до глицерина и жирных кислот.
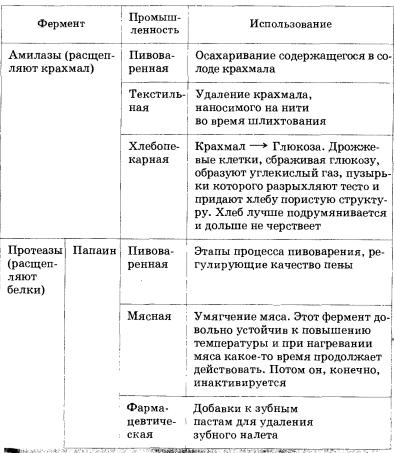
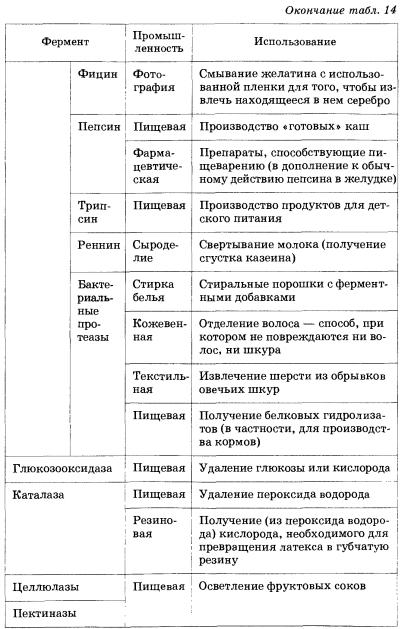
Ферменты играют немаловажную роль и в проведении многих технологических процессов. Они используются, например, в процессах приготовления пищи, в производстве пищевых продуктов и напитков, фармацевтических препаратов, моющих средств, текстиля, кожи и бумаги (табл. 14).
Таблица 14. Некоторые примеры использования ферментов в промышленности
1. Что такое ферменты? Какова их химическая природа?
2. Чем отличается действие ферментов от действия неорганических катализаторов?
3. Перечислите факторы, которые влияют на скорость ферментативной реакции.
4. При какой температуре ферменты проявляют наибольшую активность: 26 °С, 36 °С, 56 °С?
5. Укажите оптимальное значение рН для действия амилазы и пепсина.
6. Как классифицируют ферменты и как образуются их тривиальные названия?
7. Назовите области применения ферментов в промышленности.
8. Лимонную кислоту в промышленности получают при микробиологическом (ферментативном) брожении раствора глюкозы согласно уравнению
2С6Н1206 + 302 —> 2С6Н807 + 4Н20 лимонная кислота
Сколько килограммов лимонной кислоты при выходе 62% от теоретически возможного можно получить из 520 кг 15% -ного раствора глюкозы?
9. Для производства молочной кислоты путем микробиологического (ферментативного) брожения в промышленности используют крахмал и кормовую патоку. Сколько килограммов молочной кислоты при выходе 75% от теоретически возможного можно получить из 640 кг кормовой патоки, если массовая доля сухих веществ в ней составляет 80 %, из которых на долю сахарозы приходится 45%?
10*. Скорость реакции ферментативного гидролиза сахарозы не зависит от ее концентрации и прямо пропорциональна концентрации ферментов. Для экспериментального определения этой скорости 5 мл раствора сахарозы смешали с равным объемом раствора фермента и выдерживали при 25 °С в течение 30 мин, затем туда добавили избыток аммиачного раствора оксида серебра и нагрели. Выпало 0,27 г осадка. Определите время, необходимое для гидролиза при той же температуре 50% сахарозы, содержащейся в 4,68 кг ее раствора с плотностью 1,04 г/мл и массовой долей 17,1% после добавления 500 мл такого же раствора фермента.
|







